La sigla pH significa Potencial de Hidrógeno, y consiste en un índice que indica la acidez, neutralidad o alcalinidad de un medio cualquiera.
Características
El pH es una característica de todas las sustancias determinadas por la concentración de iones de hidrógeno (H +). Cuanto menor es el pH de una sustancia, mayor es la concentración de iones H + y menor la concentración de iones OH-.
Según Arrhenius, un medio que presenta hidronios es ácido, y el que presenta hidróxidos es básico. Sin embargo, debemos relacionar la cantidad de ambos iones (H + y OH-), lo que hace que la clasificación de un medio siga estos principios:
- Medio ácido: concentración de hidronios> (mayor) que la de hidróxidos.
- Medio neutro: concentración de hidronios = (igual) a de hidróxidos.
- Medio básico: concentración de hidronios < (menor) que la de hidróxidos.
Los valores de pH varían de 0 a 14, los valores por debajo de 0 y por encima de 14 son posibles, pero muy raros y no se pueden medir con los aparatos convencionales.
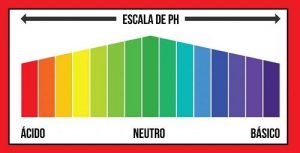
Así, podemos clasificar un medio por medio del valor del pH de la siguiente manera:
- Para pH = 7, el medio será neutro (indica que [H +] = [OH-]);
- Para pH> 7, el medio será básico (indica que [H +] < [OH-]);
- Para pH <7, el medio será ácido (indica que [H +]> [OH-]).
Las sustancias que poseen valores de pH 0 a 7, se consideran ácidas, valores en torno a 7 son neutras y valores por encima de 7 se denominan básicas o alcalinas. El pH de una sustancia puede variar según su composición, concentración de sales, metales, ácidos, bases y sustancias orgánicas y de la temperatura.
La escala del pH puede variar de 0 a 14, y cuanto menor sea el índice del pH de una sustancia, más ácida será esta sustancia.
Ejemplos
- Ácido de batería: <1,0
- Coca-Cola: 2,5
- Agua Pura: 7,0
- Saliva humana: 6,5 – 7,4
- Cloro: 12,5
El valor del pH está directamente relacionado con la cantidad de iones hidrógeno de una solución, las sustancias que revelan la presencia de iones libres en una solución se conocen como indicadores, estos cambian de color en función de la concentración de H + y de OH- en solución, es decir, del pH.
¿Cómo medir el pH?
Los llamados indicadores ácidos-base se utilizan para medir el pH de una solución. Son sustancias que cambian de color indicando el carácter de la solución. Los indicadores más utilizados son: el tornasol y la fenolftaleína.
Además de los indicadores, el pH de una solución puede medirse a través de un instrumento llamado pH-metro. Son aparatos electrónicos que miden la conductividad eléctrica de la solución y contiene una escala de los valores del pH.
Ejemplos
Soluciones Básicas
- Sangre humana
- Leche de Magnesia
- Pasta dental
- Agua de mar
Soluciones Ácidas
- Jugo gástrico
- Jugo de limón, naranja, tomate
- Leche bovina
- Café
- LLuvia ácida